스테이 바이어 (Stayveer) 란 무엇입니까?
스테이 바이어는 활성 성분 인 보센 탄을 함유 한 약입니다. 운동 용량과 증상을 개선하기 위해 3 등급의 폐 동맥성 고혈압 (PAH) 환자의 치료에 적용됩니다. PAH는 폐동맥의 압력이 높은 병리학 적 상태입니다. "등급"은 질병의 중증도를 나타냅니다. "등급 III"은 신체 활동의 엄격한 제한이 있습니다. PAH는 다음과 같습니다.
- 기본 (식별 된 또는 가족 원인 없음);
- (또는 진행성 전신 경화증, 피부 및 기타 장기를지지하는 결합 조직의 비정상적인 성장을 특징으로하는 상태);
- 선천적 인 심장 결함 (출생시 현재)과 심장과 폐 사이의 비정상적인 혈액 흐름을 일으키는 기류 (기도 기형)로 인해 발생합니다.
- PAH class II 환자에서도 개선이 관찰되었다. "클래스 II"는 신체 활동의 약간의 제한이 있습니다. 스테이 바이더는 또한 진행성 전립선 경화증을 앓고있는 성인에서 사용할 수 있는데, 이로 인해 질병으로 인한 혈액 순환 장애로 인해 "디지털 궤양"(손가락과 발가락의 염증)이 발생합니다. Stayveer의 목표는 새로운 디지털 궤양의 수를 줄이는 것입니다.
이 약은 유럽 연합 (EU)에서 이미 승인 된 Tracleer와 동일합니다. Tracleer를 만드는 회사는 자사의 과학적 데이터가 Stayveer ( "정보에 입각 한 동의")에 사용될 수 있다는 데 동의했습니다.
Stayveer - Bosentan은 어떻게 사용됩니까?
스테이 바이어는 처방전으로 만 얻을 수 있으며, PAH 또는 진행성 전립선 경화증 치료 경험이있는 의사가 치료를 시작하고 모니터링해야합니다. 스테이 바이더는 62.5mg과 125mg의 정제로 제공되며 물로 삼켜 야합니다. 태블릿은 아침과 저녁에 가져와야합니다. 성인의 경우, 시작 복용량은 4 주 동안 하루에 두 번 62.5mg이며, 이후 하루 2 회 125mg의 일반적인 복용량으로 증가합니다. PAH 소아에서 사용되는 용량은 체중에 따라 계산되어야하며 보통 1 일 2 회 킬로그램 당 2mg으로 시작해야합니다. 자세한 내용은 패키지 전단지를 참조하십시오. 의사는 Stayveer에 대한 환자의 반응을 평가하고 진행중인 디지털 궤양을 동반 한 진행성 전신성 경화증 환자에서 정기적으로뿐만 아니라 개선을보고하지 않은 PAH 환자에서 8 주 후에 추가 치료를 계속할 필요성을 판단합니다. 의사가 Stayveer로 치료를 중단하기로 결정하면 점진적으로 용량을 줄여야합니다. 스테이 바이어로 치료받는 환자에게는 의학의 안전성에 관한 주요 정보를 요약 한 특별 각서를 받아야합니다.
Stayeer - Bosentan은 어떻게 작동합니까?
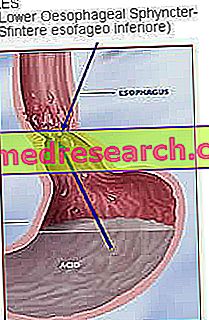
스테이 바이어의 활성 성분 인 보센 탄은 혈관을 좁히는 endothelin-1 (ET-1)이라는 자연적으로 발생하는 호르몬을 억제합니다. 따라서 스테이 바이어는 혈관 확장을 결정합니다. PAH는 폐의 혈관이 심하게 좁아지는 쇠약 병입니다. 그것은 심장의 오른쪽에서 폐로 혈액을 운반하는 혈관에서 매우 높은 혈압을 유발합니다. 이 압력은 혈액이 폐로 운반 할 수있는 산소량을 줄여 신체 활동을 어렵게 만듭니다. 이 혈관을 확장시킴으로써 혈압이 감소되고 증상이 호전됩니다. 진행성 전신 경화증과 진행중인 디지털 궤양 환자에서 bosentan은 손가락과 발가락의 혈액 순환을 개선하여 새로운 디지털 궤양의 발병을 예방합니다.
Stayveer - Bosentan이 연구 중 표시 한 이점은 무엇입니까?
PAH에서 Stayeyer는 4 가지 주요 연구에서 연구되었습니다. 1 차 또는 2 차병에서 PAH가있는 총 245 명의 성인을 대상으로 한 2 건의 연구와, 3 등급의 PAH를 지닌 54 명의 성인을 대상으로 한 연구 선천성 심장 결함, 그리고 class II에서 PAH를 가진 185 명의 환자를 대상으로 한 연구. 연구팀은 스테이 바이와 위약 (신체에 영향을주지 않는 물질)을 비교했으며, 둘 다 표준 요법에 추가됐다. 효과의 주요 척도는 환자가 6 분 (운동 능력을 측정하는 방법)으로 걸을 수있는 거리였습니다. 그러나 2 등급 질병에 대한 연구는 폐 혈관 내 혈류 저항의 변화 (혈관 수축의 지표)를 검사했다. 일차적으로 또는 경피증으로 인한 PAH class III 또는 IV에서 두 가지 연구는 Stayveer로 치료 한 환자가 16 주 치료 후 위약으로 치료 한 환자보다 더 긴 거리를 커버 할 수 있음을 보여 주었다 (연구에서 44m 이상 더 큰 크기); 그러나 IV 급의 PAH 환자 수는이 그룹에서의 의약품 사용을 지원하기에는 너무 작았습니다. 선천성 심장 결함이있는 환자에서도 비슷한 결과가 나타났습니다. Class II PAH를 가진 피험자에서, Stayeer는 6 개월 치료 후 위약에 비해 혈관 내성이 23 % 감소했지만 환자가 6 분 내에 걸을 수있는 거리는 두 그룹에서 유사했다. 3 세에서 15 세 사이의 어린이와 청소년 19 명을 대상으로 심장 및 동맥 관련 매개 변수가 개선 된 연구도 실시되었습니다. 디지털 궤양을 동반 한 진행성 전신 경화증의 경우 두 연구에서 312 명의 성인을 대상으로 스테이 바이와 위약을 비교했습니다. 효과의 주된 측정은 연구 중에 개발 된 새로운 디지털 궤양의 수에 근거합니다. 연구 중 하나는 190 명의 환자를 회복시키는 데있어 Stayveer의 효과를 관찰하여 각 환자의 특정 디지털 궤양에 대한 완전한 치유를 달성하는 데 필요한 시간을 측정했습니다. Stayveer는 새로운 디지털 궤양 형성을 줄이는데 위약보다 효과적이었습니다. 첫 번째 연구에서 스테이 바이어 (Stayveer)를 복용 한 환자는 위약으로 치료 한 환자의 2.7 궤양과 비교하여 16 주 후에 평균 1.4 개의 새로운 디지털 궤양을보고했습니다. Stayer는 24 주간의 치료 후에도 두 번째 연구에서 비슷한 결과가 관찰되었지만 디지털 궤양의 치유에는 아무런 영향을 미치지 않았습니다.
Stayeer - Bosentan과 관련된 위험은 무엇입니까?
PAH에서는 스테이 바이어 (10 명 중 1 명 이상이 영향을 미칠 수 있음)의 가장 흔한 부작용은 두통과 비정상적인 간 기능 테스트입니다. 디지털 궤양 환자에서 Stayveer (10 명 중 1 명 이상이 영향을 미칠 수 있음)의 가장 흔한 부작용은 비정상적인 간 기능 테스트, 부종 및 수분 유지입니다. 간 문제가 발생할 위험이 있으므로 의사는 치료 전 및 간병인 치료 중에 간 효소 수치를 측정합니다. Stayveer에보고 된 모든 부작용의 전체 목록을 보려면 패키지 리플릿을 참조하십시오. 스테이 바이어는 간 문제가있는 환자, 임신 중이거나 출산 연령이 높은 여성, 믿을 수없는 피임법을 사용하지 않는 환자 또는 면역 억제제 인 사이클로스포린 A로 치료받은 환자에게 사용하면 안됩니다. 제한 사항의 전체 목록은 패키지 소책자를 참조하십시오.
Stayveer - Bosentan이 승인 된 이유는 무엇입니까?
기관의 의약품 사용위원회 (CHMP)는 Stayveer의 이익이 위험보다 크며 EU에서의 사용 승인을 권고했습니다.
Stayeer - Bosentan의 안전하고 효과적인 사용을 보장하기 위해 취하는 조치는 무엇입니까?
Stayveer가 가능한 한 안전하게 사용되도록 위험 관리 계획이 수립되었습니다. 이 계획에 따라 건강 관리 전문가와 환자가 따라야 할 적절한주의 사항을 포함하여 제품 특성의 요약과 Stayveer의 패키지 전단에 안전 정보가 포함되었습니다. 또한, Stayveer를 만드는 회사는 Stayveer의 안전성을 설명하기 위해 처방자를위한 정보 키트와 각 회원국의 환자를위한 정보 전단을 제공 할 것입니다 (특히 간 및 임신 중에 미치는 영향과 관련하여). 그의 상호 작용. 이 회사는 또한 각 회원국의 의약품 배포를주의 깊게 모니터링하고 디지털 궤양 진행중인 진행성 전신성 경화증 환자에 대한 사용 정보를 수집하기로 약속합니다.
Stayveer - 보센 탄에 대한 상세 정보
2013 년 6 월 24 일 유럽 집행위원회 (European Commission)는 유럽 연합 (EU) 전역에서 유효 기간 동안 유효한 마케팅 허가를 부여했습니다. 스테이 바이어 치료에 대한 더 자세한 정보는 소책자 (EPAR의 일부 임)를 읽거나 의사 또는 약사에게 문의하십시오. 이 요약의 최종 업데이트 : 06-2013.