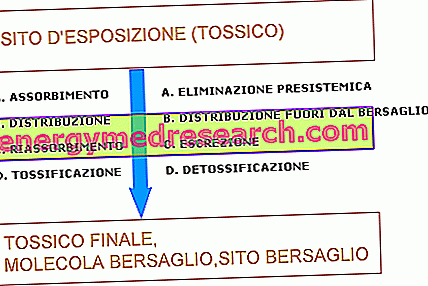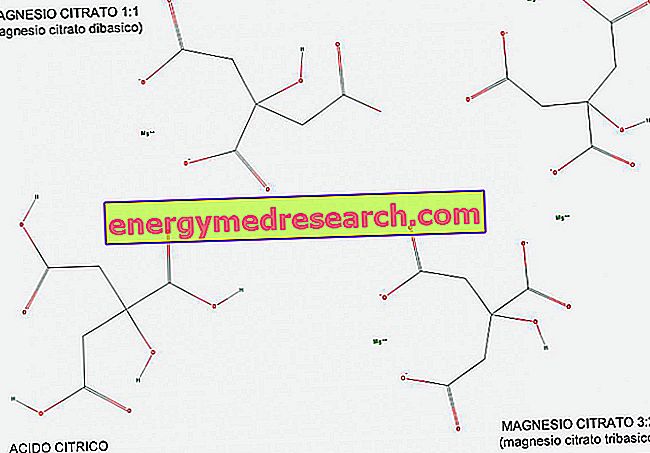
삼 염기성 (또는 삼 염성) 산은 산 - 염기 반응에서 기증 할 3 개의 수소 이온을 갖는 산이다. 그림의 도움으로 우리는 구연산이 쉽게 수소 H를 전달할 수있는 3 개의 COOH 카르복실기를 갖기 때문에 어떻게 삼산화탄산의 예가되는지 볼 수 있습니다.
마그네슘 구연산염은 1 : 1 비율 (구연산염 분자 당 1 마그네슘 분자) 및 3 : 2 비율 (구연산염 2 분자 당 3 마그네슘 분자)로 존재합니다.
1 : 1의 마그네슘 구연산염은 구연산의 이염 기성 염이기 때문에 이염이라고 불립니다. 실제로 그것은 반응 동안 수소를 포기한 2 개의 카르복실기로부터 유도 된 분자 당 2 개의 1가 염기성 기 (COO-)를 갖는다.
3 : 2 마그네슘은 반응 중에 수소를 포획 한 3 개의 카르복실기에서 유래 한 1 분자 당 3 개의 1가 염기성 기 (COO-)를 가지고 있기 때문에 3 차 전지라고 불립니다.
삼 염기성 마그네슘 구연산염은 마그네슘 (+ 42.6 중량 %)이 이염 기성 마그네슘 구연산염보다 분명히 풍부하다. 또한, 그것은 더 많은 알칼리성이며, 이는 이염기에 의해 수용되는 2 개의 수소 이온에 대하여 3 개의 수소 이온 H +를 수용 할 수 있기 때문이다. 그러나 물에 덜 녹습니다.